cmde产品注册图解与国内旅游业务解析
cmde(国家药品监督管理局医疗器械技术审评中心)产品注册是医疗器械上市前的重要环节,其流程涉及资料准备、技术审评、体系核查等多步骤。本文结合图解与国内旅游业务背景,解析医疗器械注册要点及行业应用。
一、cmde产品注册流程图解(两则)
1. 注册申请流程图解
- 第一阶段:产品分类与路径确认
图示:产品分类决策树(按风险等级分为I、II、III类)
说明:企业需根据《医疗器械分类目录》确定产品管理类别,选择对应注册路径(如备案或申报注册)。
- 第二阶段:资料准备与提交
图示:资料清单与提交流程(含技术文件、临床评价、质量管理体系文件等)
说明:需提交产品技术要求、检验报告、临床评价资料等至cmde,并完成电子申报。
- 第三阶段:技术审评与补充资料
图示:审评环节交互流程(含受理、补正、专家评审等节点)
说明:cmde对资料进行审核,可能发出补正通知,企业需及时响应。
- 第四阶段:体系核查与审批发证
图示:现场核查与证书颁发流程
说明:通过审评后,cmde组织生产体系核查,合格后颁发医疗器械注册证。
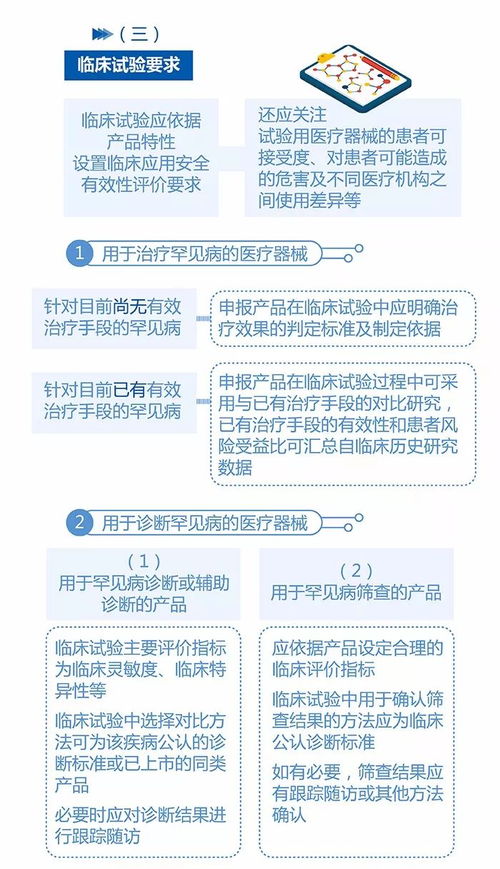
2. 临床评价路径图解
- 路径一:同品种比对
图示:数据对比与证据链构建流程
说明:通过已有同类产品数据证明安全有效性,需提供比对分析报告。
- 路径二:临床试验
图示:临床试验申请与实施流程(含伦理审查、中心选择、数据统计)
说明:高风险产品需开展临床试验,提交试验方案和报告至cmde。
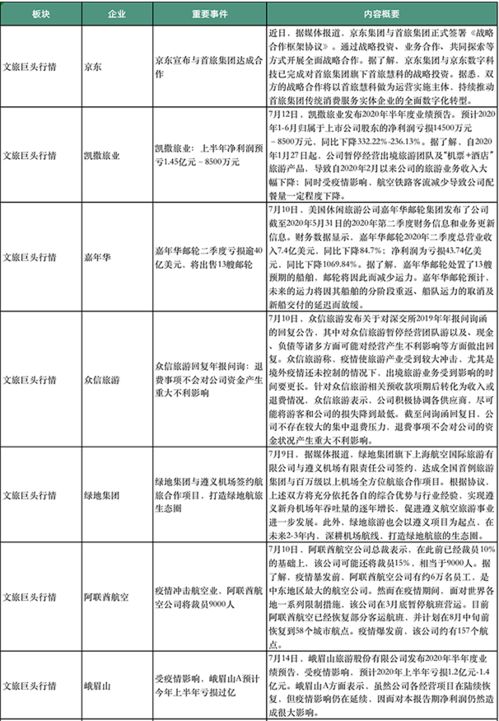
二、国内旅游业务中的医疗器械注册关联
随着国内旅游业的复苏,便携式医疗器械(如血糖仪、血压计)需求增长,其注册合规性成为业务拓展关键:
- 旅游健康服务应用:旅行社与健康机构合作时,需确保所用设备具有效注册证,避免法律风险。
- 地域适应性:不同省份对医疗器械监管存在差异,企业需结合旅游目的地政策调整注册策略。
- 创新产品案例:例如可穿戴健康监测设备,在注册时需重点说明其在旅游场景下的稳定性与数据可靠性。
cmde注册流程的规范化保障了医疗器械安全,企业应结合图解深入理解各环节,同时在旅游业务中强化合规管理,推动产品与服务的协同发展。
如若转载,请注明出处:http://www.gacy158.com/product/46.html
更新时间:2025-11-29 02:46:50